- Reducir la exposición a las Lutzomyia es la mejor defensa contra la Leishmaniasis cutánea y otras infecciones transmitidas por vectores. A nivel individual y familiar se pueden tomar varias medidas para prevenir y controlar la Leishmaniasis cutánea:
- La exposición a las Lutzomyia puede ocurrir durante todo el año, pero las Lutzomyia son más activas durante los meses más secos (febrero – marzo/ noviembre-diciembre).
- Antes de salir al aire libre, zona boscosa o selvática
- Sepa dónde esperar las Lutzomyia. Las Lutzomyia viven en áreas cubiertas de material orgánico, huecos en troncos de árboles, desechos vegetales acumulados, por debajo de los 1400 msnm de altura. Exponerse en horas de la noche, al atardecer o al amanecer podría ponerlo en contacto cercano con las Lutzomyia. Muchas personas son picadas incluso durante la recolección de las cosechas.
- Use la ropa que proteja la piel expuesta: Las Lutzomyia miden entre 3 y 4 mm, por lo tanto, no pueden atravesar la ropa. El uso de camisas o buzos de manga larga, pantalón de manga larga, protege las partes más expuestas a la picadura de la Lutzomyia
- Use repelentes de insectos; utilice los repelente comercialmente disponibles para proteger la piel de la cara y las manos, que quedan expuestas.
- Evite el contacto con las Lutzomyia
- Evite las áreas boscosas y selváticas.
- Trabajar siempre con ropa protectora.
Los pasos para prevenir la Leishmaniasis cutánea incluyen usar repelente de insectos, usar ropa de manga larga para proteger la piel expuesta, usar toldillo que bloquea la picadura, especialmente durante el reposo. Capacitación laboral con énfasis en protección y promoción del diagnóstico presuntivo. (Organización Panamericana de la Salud. Manual de procedimientos para vigilancia y control de las leishmaniasis en las Américas. Washington, D.C.: OPS; 2019
¿Cuáles son las condiciones de vida de los pacientes que los pone en riesgo?
Vivienda: las condiciones de la vivienda que permiten la cría del vector, al acumular material orgánico al interior o en el peridomicilio, cercanía al bosque o la selva Paredes con agujeros que permitan el ingreso de insectos al interior de la vivienda.
El no uso de anjeos o cortinas que limiten el ingreso de insectos, al igual que el no uso de toldillo impregnado de insecticida. Permitir que los niños duerman sin toldillo.
Laboral: Actividades que se desarrollan en el bosque o la selva, como trabajadores de la construcción de carreteras, mineros, pescadores, militares, cazadores, cultivadores y colonos.
Recreativo: Realizar actividades como cacería o pesca en la noche, en áreas boscosas y selváticas sin protección.
(Organización Panamericana de la Salud. Manual de procedimientos para vigilancia y control de las leishmaniasis en las Américas. Washington, D.C.: OPS; 2019)
Prevención de las Lutzomyia en la vivienda y sus alrededores
- Cree una zona segura contra las Lutzomyia.
- Limpie los pastos altos y mantenga despejada el área alrededor de las casas y en los bordes del césped.
- Apile la madera ordenadamente y en un área seca (desalienta a los roedores de los que se alimentan las Lutzomyia).
- Retire todos los muebles viejos, colchones o basura del jardín que puedan darles a las Lutzomyia un lugar para esconderse. Manejo de residuos orgánicos alejado de las viviendas al menos 300 metros. Promoción del saneamiento ambiental Mejoramiento de las condiciones de vivienda.
¿Existen riesgos en la comunidad o en la familia si hay otras personas con las mismas lesiones?
La transmisión entre humanos no se ha demostrado, por lo tanto, la presencia de otras personas con lesiones por LC, no representa riesgo para la familia o la comunidad. Lo importante es determinar dónde se han infectado y evitar llegar a esas zonas sin protección.
(Organización Panamericana de la Salud. Manual de procedimientos para vigilancia y control de las leishmaniasis en las Américas. Washington, D.C.: OPS; 2019)
¿Los animales pueden presentar la enfermedad y transmitirla al humano?
La leishmaniasis cutánea puede generar lesiones ulceradas en los animales domésticos (perro, caballo), sin embargo, no se ha demostrado que estas lesiones sean fuente de infección para la Lutzomyia y pueda generar infección en humanos
(Organización Panamericana de la Salud. Manual de procedimientos para vigilancia y control de las leishmaniasis en las Américas. Washington, D.C.: OPS; 2019)
¿Los tratamientos caseros han mostrado que mejoran los pacientes?
La LC, tiene una proporción de casos con curación espontánea y tratamientos caseros basados en calor local pueden generar resolución espontánea de las lesiones.
¿Cuáles son las formas de prevención colectiva?
- Participar eficazmente en programas de promoción de la salud y adoptar hábitos saludables
- Recibir adecuadamente información para el aprendizaje y cambio significativo
- Consultar en forma regular a profesionales de la salud.
- Buscar información y adoptar hábitos protectores
¿Cuáles son las formas de prevención comunitaria?
- Manejo de residuos orgánicos alejado de las viviendas al menos 300 metros.
- Capacitación laboral con énfasis en protección.
- Promoción del saneamiento ambiental
- Mejoramiento de las condiciones de vivienda.
- Promoción del diagnóstico presuntivo
¿Cuáles son las formas de prevención secundaria y terciaria?
Prevención Secundaria
- Diagnóstico presuntivo en el contexto comunitario.
- Búsqueda precoz de atención médica.
- Confirmación diagnóstica de laboratorio temprana.
- Acceso precoz a tratamientos locales menos invasivos.
- Detección temprana de potencial toxicidad de los medicamentos
Prevención Terciaria
- Detección precoz de complicaciones mucosas.
- Remisión oportuna a nivel de mayor complejidad.
- Identificación y detección temprana de falla terapéutica
¿Qué es diagnóstico presuntivo y en qué consiste?
El diagnóstico presuntivo es la detección precoz de una enfermedad o condición, tratando de estimular el diagnóstico y tratamiento precoz y evitar las complicaciones. Basados en la regla de predicción se pueden tener en cuenta estos seis elementos para hacer un diagnóstico presuntivo en LC:
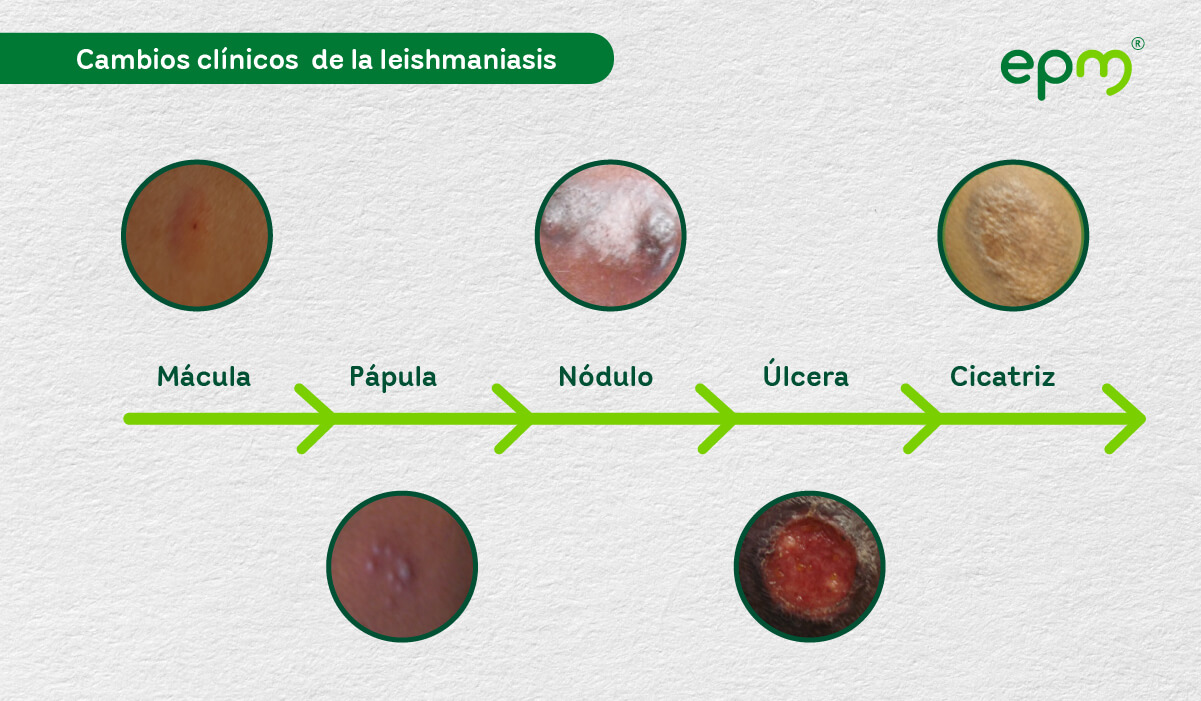
- Úlceras de bordes gruesos, forma redondeada u ovalada
- Aparición de lesiones especialmente en brazos, piernas y cara, aunque puede presentarse en cualquier parte del cuerpo expuesta a la picadura de la mosca
- Lesiones únicas o separadas al menos 10 cm unas de otras.
- Exposición a bosques o selvas por más de cuatro horas al amanecer, el anochecer y en la noche
- No presentar antecedentes de trauma, quemadura o cortadura en la lesión.
- Reconocer haber estado en contacto con la mosca o flebótomo (Lutzomyia).
(Weigle KA, Escobar M, Arias AL, Martinez F, Rojas C. A clinical prediction rule for American cutaneous leishmaniasis in Colombia. Int J Epidemiol. 1993 Jun;22(3):548-58. doi: 10.1093/ije/22.3.548. PMID: 8359974).